€ 5.0890 →
|
$ 4.3140 →
|
 Imagine de Tumisu de la Pixabay
Imagine de Tumisu de la Pixabay
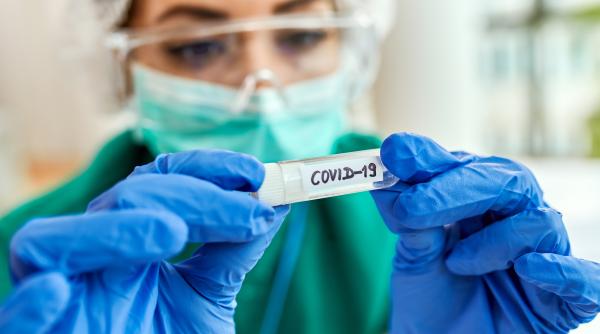
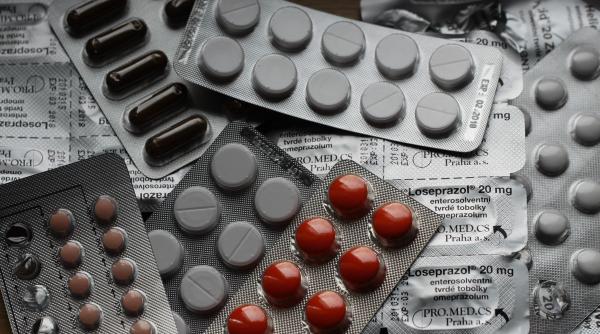
Paxlovid, medicamentul experimental antiviral împotriva COVID-19 dezvoltat de Pfizer, reduce cu 89% riscul de spitalizare sau deces, a anunțat compania.
Compania Pfizer a anunțat vineri, într-un comunicat de presă, că medicamentul antiviral Paxlovid, aflat momentan în teste clinice de fază 3, reduce riscul de spitalizare sau deces cu până la 89%. Anunțul Pfizer a venit la scurt timp după autorizarea Monupiravir în Marea Britanie.
Rezultatele par să le depășească pe cele observate la pastila Molnupiravir de la Merck & Co Inc, despre care s-a demonstrat luna trecută că reduce la jumătate riscul de spitalizare sau deces.
CEO-ul companiei Pfizer, Albert Bourla, a declarat vineri că rezultatele studiilor de fază 2/3 sunt foarte promițătoare. Compania Pfizer va depune documentația necesară pentru aprobarea în regim de urgență a medicamentului antiviral Paxlovid de către Autoritatea americană a medicamentului (FDA).
Mai puțin de 1% dintre pacienții cărora le-a fost administrat medicamentul au avut nevoie de spitalizare. Compania Pfizer a precizat că aproximativ 0,8 dintre pacienții care au primit combinația de medicamente au fost spitalizați în decurs de o lună, respectiv 3 din 389 de pacienți. 7% dintre pacienții cărora li s-a administrat placebo, respectiv 27 din 385 au fost spitalizați.
Niciun participant infectat care a fost tratat cu Paxlovid nu a decedat, a precizat Albert Bourla.
Studiul a fost realizat pe 775 de adulți cu Covid-19, considerați cu risc crescut de a dezvolta o formă severă. Participanților li s-a administrat aleatoriu fie o combinație de medicamente, fie placebo, la trei sau cinci zile de la debutul simptomelor.
Agenția de reglementare a medicamentelor (MHRA) a recomandat ca pastila să fie folosită cât mai curând posibil după un test COVID-19 pozitiv și în termen de cinci zile de la apariția simptomelor, conform Reuters.
Este primul tratament antiviral oral pentru COVID-19 care a fost aprobat, iar unda verde a fost dată înainte de o eventuală autorizare din partea autorităților americane.
Medicamentul, care va fi denumit Lagevrio în Marea Britanie, a fost urmărit îndeaproape după ce datele de luna trecută au arătat că ar putea reduce la jumătate riscul de deces sau de spitalizare pentru bolnavii COVID-19, dacă este administrat la începutul bolii.
Guvernul britanic și Serviciul Național de Sănătate din această țară vor confirma în timp util modul în care tratamentul va fi aplicat pacienților.
Luna trecută, Marea Britanie a încheiat un acord cu Merck pentru a asigura 480.000 de doze de molnupiravir, notează Mediafax.
Compania Merck a anunţat, în urmă cu trei săptămâni, că a depus la Agenţia pentru Alimente şi Medicamente din Statele Unite o cerere de autorizare în regim de urgenţă a pastilei sale anti-COVID-19. Potrivit unui studiu clinic, medicamentul reduce cu aproximativ 50% riscul de spitalizare şi de deces pentru pacienţii diagnosticaţi cu această boală.
Fiți la curent cu ultimele noutăți. Urmăriți DCNews și pe Google News



































































 Fiat Justitia, pereat mundus-adevăratul înțeles al expresiei care justifică protestele din Piața Victoriei
Fiat Justitia, pereat mundus-adevăratul înțeles al expresiei care justifică protestele din Piața Victoriei
de Val Vâlcu

